Kadcyla赫赛莱Trastuzumab Emtansine恩美曲妥珠单抗详细说明书及完整处方信息
一、药品基本信息
中文通用名:恩美曲妥珠单抗
英文通用名:Trastuzumab Emtansine
商品名:Kadcyla®(赫赛莱®)
研发代号:T-DM1
生产厂家:罗氏制药(Roche Pharma (Schweiz) AG)
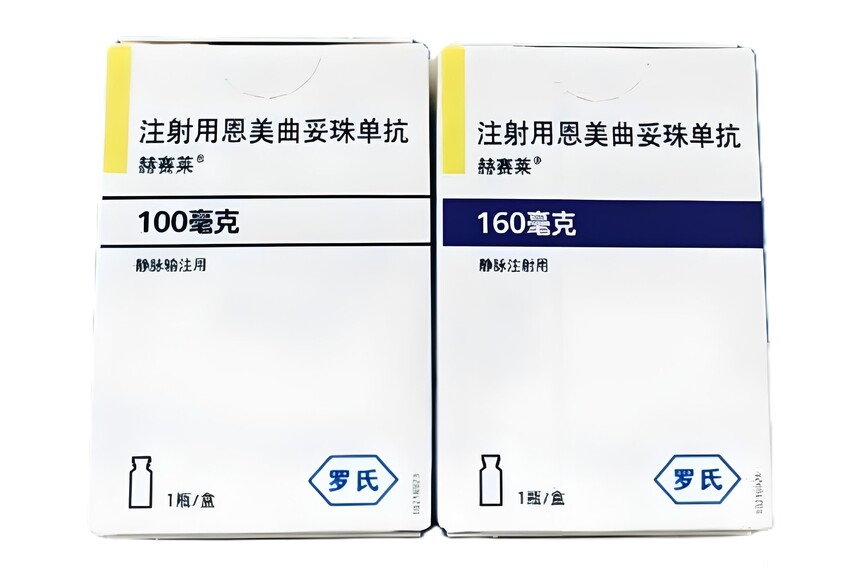
剂型规格:冻干粉制剂,100 mg/瓶或160 mg/瓶
分子量:约148,781 Da
辅料:琥珀酸、氢氧化钠、聚山梨酯20、蔗糖
二、靶点与作用机制
靶点:HER2(人表皮生长因子受体-2)
作用机制:
抗体部分:人源化抗HER2 IgG1单克隆抗体(曲妥珠单抗),特异性结合HER2阳性肿瘤细胞表面。
连接子:稳定硫醚连接体(MCC),在肿瘤细胞内被酶解,释放细胞毒性载荷。
载荷:微管抑制剂DM1(美坦辛衍生物),抑制微管聚合,阻断细胞分裂,诱导肿瘤细胞凋亡。
旁观者效应:DM1可穿透肿瘤细胞膜,杀伤邻近HER2阴性肿瘤细胞。
三、适应症
HER2阳性乳腺癌:
既往接受过针对不可切除或转移性疾病的内分泌治疗和化疗;
或完成辅助治疗期间或6个月内疾病复发。
不可切除或转移性、激素受体(HR)阳性/阴性(IHC 3+或IHC 2+/ISH+)的成年患者,需满足:
新辅助治疗后未达病理完全缓解(pCR)的HER2阳性早期乳腺癌患者的辅助治疗。
HER2突变型非小细胞肺癌(NSCLC):
局部晚期或转移性EGFR突变型NSCLC,经EGFR靶向治疗和含铂化疗后进展。
四、用法用量
推荐剂量:6 mg/kg,每3周(21天周期)静脉输注一次,直至疾病进展或出现不可耐受毒性。
给药方式:
首次减量至4.5 mg/kg,第二次减量至3 mg/kg;若仍不耐受,永久停药。
延迟给药:尽快补输,后续周期维持3周间隔。
首次输注:≥60分钟,观察发热、寒战等反应。
后续输注:若耐受良好,可缩短至30分钟,仍需观察反应。
剂量调整:
特殊人群:
轻度/中度肾功能不全:无需调整剂量;重度肾功能不全数据有限。
轻度/中度肝损害:无需调整剂量;重度肝损害未研究,谨慎使用。
老年人(≥65岁):无需调整剂量。
五、副作用与不良反应
常见不良反应(≥25%):
血液学:血小板减少、贫血、中性粒细胞减少。
胃肠道:恶心、便秘、呕吐。
全身:疲劳、头痛、周围神经病变。
实验室异常:转氨酶升高、低钾血症。
严重不良反应:
间质性肺病(ILD)/肺炎:发生率约2%-3%,可能导致死亡。
肝毒性:肝衰竭、结节性再生性增生(NRH),需监测肝功能。
心脏毒性:左心室射血分数(LVEF)下降,需定期评估心功能。
胚胎-胎儿毒性:可能导致胎儿死亡或先天缺陷,育龄期女性需有效避孕。
六、临床治疗效果
HER2阳性乳腺癌:
中位无进展生存期(PFS):6.9个月(化疗组4.9个月),疾病进展或死亡风险降低37%(HR=0.63)。
中国亚组数据:中位PFS 8.1个月(化疗组4.2个月),ORR 38.6%(化疗组17.9%)。
TROPION-Breast01研究:
HER2突变型NSCLC:
ORR 43.6%,中位PFS 5.4个月,中位总生存期(OS)13.6个月。
TROPION-Lung05研究:
七、注意事项
监测要求:
输注期间密切观察发热、寒战等反应,严重者暂停或永久停药。
定期监测肝功能(血清转氨酶、胆红素)、心功能(LVEF)、血小板计数。
特殊人群:
育龄期女性:治疗期间及末次给药后6个月内采取有效避孕措施。
哺乳期女性:暂停哺乳。
药物相互作用:
避免与强效CYP3A4抑制剂(如酮康唑)或诱导剂(如利福平)联用。
操作规范:
复溶后溶液需在2-8℃冷藏,24小时内使用;稀释后溶液需在4小时内输注完毕。
禁止使用葡萄糖溶液稀释,需用0.9%氯化钠注射液。
八、完整处方信息
成分:活性成分trastuzumab emtansine,辅料包括琥珀酸、氢氧化钠等。
性状:白色至类白色无菌冻干粉饼。
贮藏:未复溶样品瓶2-8℃冷藏,复溶后溶液2-8℃冷藏不超过24小时。
包装:西林瓶,1瓶/盒。
有效期:36个月(具体以包装标注为准)。
执行标准:进口注册标准JS20160063。
批准文号:进口药品注册证号S20200002、S20200003。
九、医保情况与价格
医保覆盖:已纳入国家医保目录(乙类),适应症包括HER2阳性乳腺癌辅助治疗及晚期治疗。
价格:未公开具体定价,参考同类ADC药物年治疗费用约50万-100万元人民币,具体以医院或药房公示为准。
推荐
-

-

QQ空间
-

新浪微博
-

人人网
-

豆瓣









